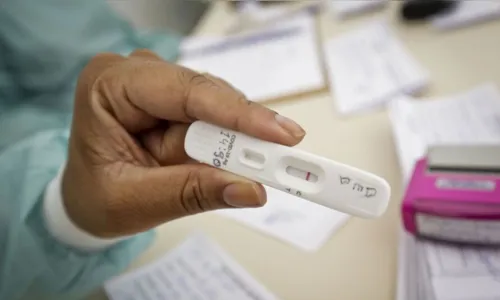
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou na última sexta-feira (28) a distribuição, comercialização, registro e utilização de autotestes para Covid-19 no país em reunião da Diretoria Colegiada. Até a última sexta-feira (4), 24 empresas haviam feito 30 pedidos de registro ao órgão.
Agora, a Gerência Geral de Tecnologia em Produtos para Saúde (GGTPS) tem até 30 dias para analisar as solicitações. A expectativa é de que os autotestes só estejam disponíveis para a população a partir de março.
LEIA TAMBÉM:
Tiroteio termina com morte de mais um suspeito de matar PM
Segundo o presidente da Câmara Brasileira de Diagnóstico Laboratorial (CBDL), Carlos Eduardo Gouvêa, a expectativa é de que uma embalagem unitária tenha o custo entre 45 e 70 reais. “A gente espera que seja bem abaixo do teste rápido de antígeno profissional, que tem o acréscimo de valor por causa do serviço de apoio farmacêutico ou laboratorial”, destaca.
Os pedidos de registros que aguardam avaliação na Anvisa utilizam a coleta de saliva ou nasal, feita por meio do swab, uma espécie de cotonete. Os testes serão vendidos em estabelecimentos comerciais, como farmácias, e por enquanto, não distribuídos pelo Sistema Único de Saúde (SUS).
Os autotestes não serão utilizados como definidores de diagnóstico, que devem ser confirmados por um profissional de saúde. Eles também não são válidos como comprovante para viagens ou acesso a eventos.